294: 注射體(Injectisome)
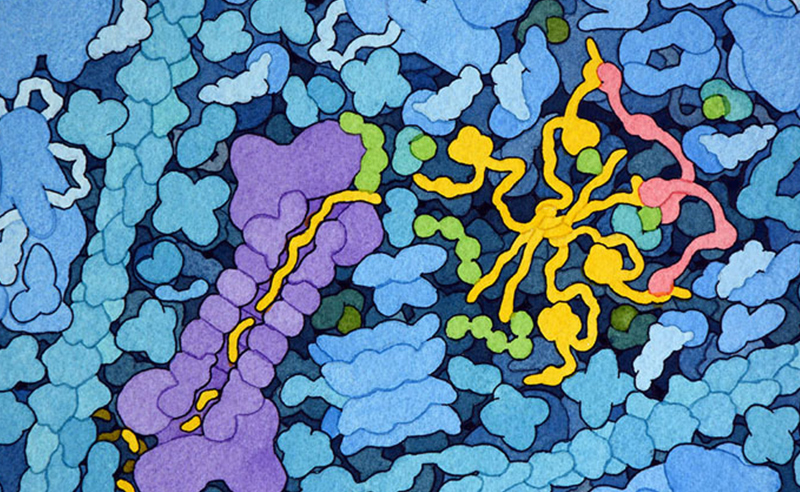
我們與許多細菌共生,我們與它們的互動通常是友好的。環境中的細菌會分解廢物和死去的動植物。我們體內的細菌可以幫助我們處理所吃的食物,為我們提供所需的營養。不過,有時也會有不那麼友善的互動。例如,沙門氏菌(Salmonella bacteria)會侵入我們的細胞並在內部繁殖,從而引發傷寒(typhoid fever)等危及生命的疾病。作為其致病策略的一部分,這些細菌利用名為注射體( injectisome)的針狀分子注射數十種不同的效應蛋白。這些注入的蛋白質會使細胞防禦失活,並改寫細胞的新陳代謝,以幫助細菌在細胞內生長。
注射效應器
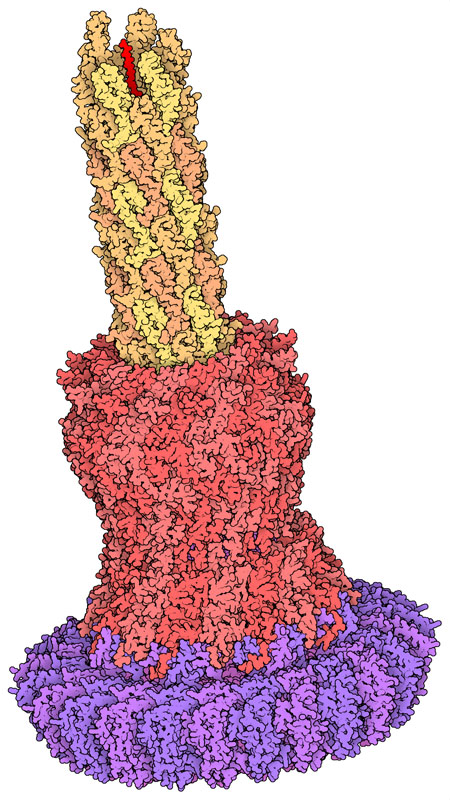
PDB 條目7ah9包含注射體沙門氏菌注射體的中心針狀部分,其針頭中間有一個孔,孔的大小剛好可以容納一條未折疊的蛋白質鏈。一個分子門控制效應蛋白通過針頭,下面的互動式可操作圖像詳細顯示了這個分子門。該結構還包含幾個大的環形蛋白,它們將針頭固定在細菌細胞壁上,使細菌能夠將多個針頭放置在它試圖感染的細胞上。
完整的注射體還包含一個位於細菌內部的大型分類平台,此平台的結構沒有包含在這個PDB條目中。該平台只選擇適當的效應蛋白,並控制它們的注射順序。它們的分泌過程分為三個階段。首先,分泌注射體本身,以產生針頭等成分。其次,分泌一組蛋白質,製造穿透受感染細胞膜的轉位子(translocon)。最後,注射體與此轉位子結合,將剩餘的效應蛋白注入受感染細胞的細胞質中。
凍結活動
注射體的結構是透過冷凍電子顯微鏡確定的,其中含有效應蛋白SptP,這種酶可以去除細胞蛋白質中酪胺酸的磷酸鹽,還能使幾種受GTP 調節的蛋白質失去活性。在觀察蛋白質的運送過程中需要一些巧妙的方法。這是因為效應蛋白通過針頭的時間通常不到一秒鐘。具體來說,我們在SptP 的末端加入了綠色熒光蛋白(green fluorescent protein、GFP)。注射體無法解開GFP的折疊,因此起到了鉗子的作用,使其無法通過針孔,從而可以緩慢地捕獲和研究複合物。
有效的效應器
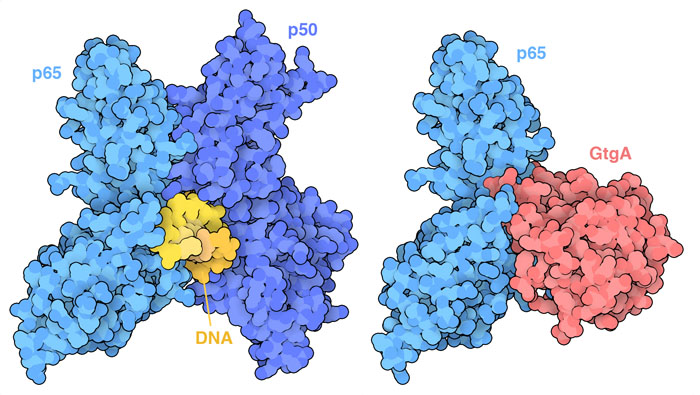
沙門氏菌會注入數十種不同的效應蛋白。其中許多會添加或去除磷酸鹽、核糖基團和其他化學修飾,從而阻止細胞蛋白質發揮作用。另一組效應蛋白會將關鍵的細胞蛋白質送到泛素化系统(ubiquitination system)進行處理。圖中所示的效應蛋白GtgA是一種蛋白酶,它能裂解特定的轉錄因子p65(PDB條目6ggr),此轉錄因子是NF-κB訊號路徑的一部分,圖中所示的NF-κB 複合物是p65和p50(PDB 條目1le5)與DNA 結合的異二聚體。
探索結構
若要切換到有互動控制的頁面,請點擊圖表下方的按鈕。如果載入沒有開始,請嘗試點擊圖表。
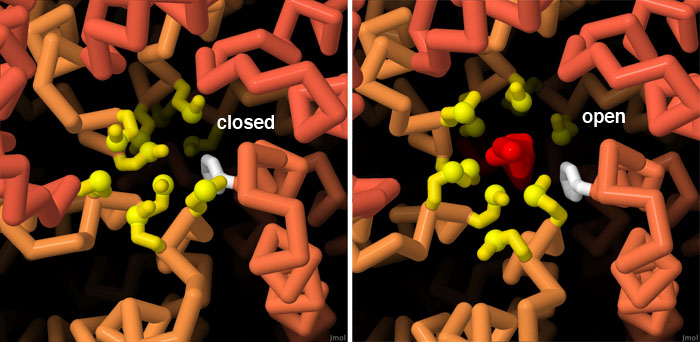
分泌針的入口受到蛋氨酸門(methionine gate)的保護,如PDB 6pep所示,當分泌針不使用時,蛋氨酸群(黃色)得到單一苯丙胺酸(白色)的幫助,形成防水屏障。之後,一旦確定了要注入細胞的效應蛋白,蛋胺酸就會順利分離,讓細蛋白鏈(紅色)通過,如PDB 7ah9所示。點擊螢幕下方的按鈕,切換到互動式可操作圖像,更詳細地查看這兩種結構。
進一步的討論議題
- 搜尋" 沙門氏菌效應蛋白"(Salmonella effector),查看由注射體運輸的該效應蛋白和其他效應蛋白的結構。
- 針狀複合體包含幾個對稱的環狀結構,由一種蛋白質的多個拷貝組成。
參考文獻
- 2023 Speaking the host language: how Salmonella effector proteins manipulate the host. Microbiology 169 001342
- 7ah9 2021 Substrate-engaged type III secretion system structures reveal gating mechanism for unfolded protein translocation. Nat Commun 12 1546
- 6pep 2019 T3S injectisome needle complex structures in four distinct states reveal the basis of membrane coupling and assembly. Nat Microbiol 4 2010-2019
- 6ggr 2018 Structure-function analyses of the bacterial zinc metalloprotease effector protein GtgA uncover key residues required for deactivating NF-kappa B. J Biol Chem 293 15316-15329
- 1le5 2002 The X-ray crystal structure of the NF-kB p50/p65 heterodimer bound to the Interferon beta-kB site. J Biol Chem 277 24694-24700
 生物大分子學習的教育門戶
生物大分子學習的教育門戶