298: 血管緊張素和血壓(Angiotensin and Blood Pressure)
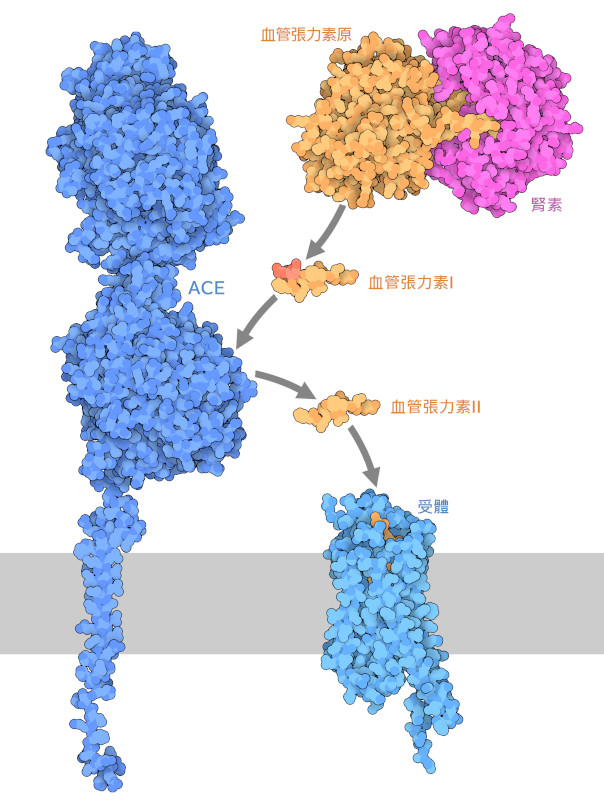
保持健康的血壓需要一種微妙的平衡。血壓必須保持足夠高的水平,以便讓血液循環到全身,但又不能過高,以免造成傷害。我們的身體會不斷監測血壓,並在血壓超出最佳範圍時做出改變。荷爾蒙血管緊張素(angiotensin)在這種控制中扮演核心角色。當血壓需要升高時,就會分泌這種荷爾蒙。血管緊張素會在體內流動,並產生一系列影響,包括收縮血管和使我們感到口渴。
發出訊號
血管緊張素透過幾個階段發揮其功能。血管緊張素在肝細胞中生成一種稱為血管緊張素原(angiotensinogen)的大型非活性前體,在需要時釋放到血液中。腎臟同時釋放出一種小型蛋白酶腎素(renin),它可以切除部分血管緊張素原,生成一種名為血管緊張素I的小型十肽(10 個殘基的勝肽)。然後,ACE(血管緊張素轉換酶,angiotensin-converting enzyme)又將血管緊張素I 剝離出兩個胺基酸,形成八肽(8 個殘基的勝肽),即血管緊張素II。血管張力素II 是一種活性荷爾蒙,可與全身細胞表面的受體結合,啟動一系列過程,控制水和鹽的流動,釋放更多荷爾蒙並收縮血管。
血管張力素的作用
我們可以在PDB 檔案中探索這些分子的分子細節。從下圖所示的可操作互動式圖表中可以看到,腎素的非活性前體(PDB ID 3vcm)的結構可以與切割血管緊張素原的活性形式(PDB ID 2x0b)的結構進行比較。它有兩個類似的蛋白質裂解結構域,可裂解勝肽類激素。此處顯示的整體結構是透過計算得出的結構模型( AF_AFP12821F1 ),但PDB 檔案中提供了許多透過實驗解析的單一結構域結構。血管張力素I 的結構(PDB ID 1n9u)和與血管張力素II 結合的受體結構(PDB ID 6os0)也可在PDB 中找到。
降血壓藥
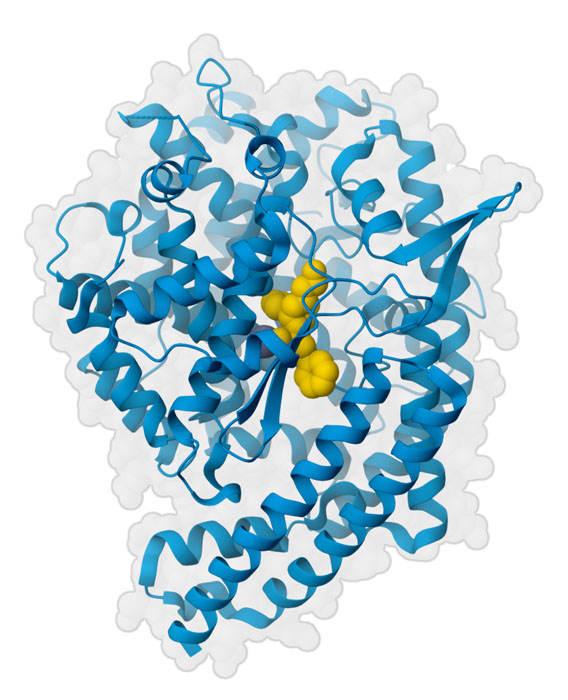
對參與血管緊張素訊號通路的蛋白質結構的了解,促進了改變其作用並在必要時降低血壓的藥物的開發。這裡顯示的是廣泛使用的賴諾普利(lisinopril),它與ACE 的血管緊張素裂解結構域的活性位點結合(PDB ID 1o86)。由於血壓控制對健康非常重要,因此也開發了抑制訊號通路中其他步驟的藥劑。例如,下一節所示的可操作互動式圖表中就包含抑制腎素作用的製劑。
探索結構
若要切換到有互動控制的頁面,請點選圖表下方的按鈕。如果載入沒有開始,請嘗試點擊圖表。
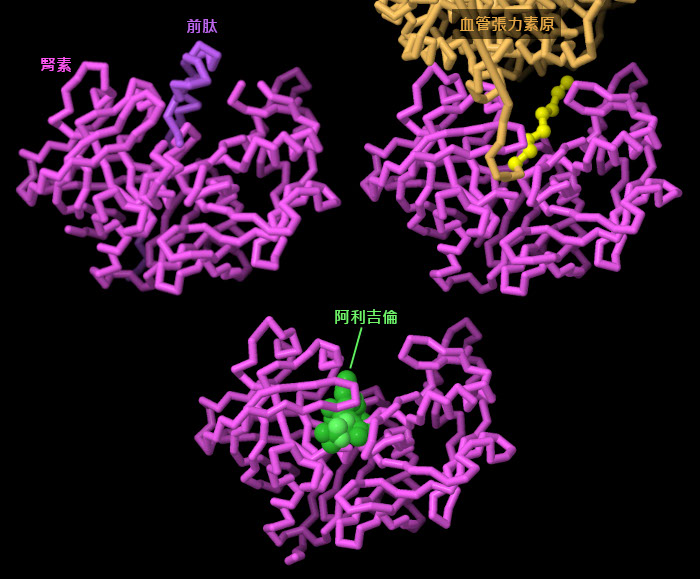
這三種結構揭示了腎素的不同狀態:PDB ID 3vcm結構包含腎素的非活性形式,它是在腎臟細胞中製造的。 PDB ID 2x0b的結構顯示了腎素如何與血管緊張素原結合併將其放置在正確的位置,以便在正確的位置被裂解。 PDB ID 2v0z的結構顯示了藥物阿利吉崙(Aliskiren)與活性位點的結合,該藥物可抑制腎素的作用並幫助降低血壓。
點擊圖表底部的按鈕,切換到互動式可操作圖像,更詳細地查看這些結構。
進一步的討論議題
- ACE2 與此處描述的ACE 相似,可進一步裂解血管張力素。 SARS-CoV-2 也使用ACE2 作為感染受體。其結構請參考PDB ID 6m17。
- 使用RCSB PDB 的配對結構比對工具,可以比較兩個ACE 結構域,每個結構域的PDB ID分別為1o86 和2c6n 。
參考文獻
- 2024 Physiology, Renin Angiotensin System. StatPearls www.ncbi.nlm.nih.gov/books/NBK470410/
- 6os0 2020 Angiotensin and biased analogs induce structurally distinct active conformations within a GPCR. Science 367 888-892
- 2013 A modern understanding of the traditional and nontraditional biological functions of angiotensin-converting enzyme. Pharmacol Rev 65 1-46
- 2x0b 2010 A redox switch in angiotensinogen modulates angiotensin release. Nature 468 108
- 1o86 2003 Crystal structure of the human angiotensin-converting enzyme-lisinopril complex. Nature 421 551
- 1n9u 2003 Comparison of the solution structures of angiotensin I & II. Implication for structure-function relationship. Eur J Biochem 270 2163-2173
- 2v0z 2000 Structure-based drug design: The discovery of novel nonpeptide orally active inhibitors of human renin. Chem Biol 7 493-504
 生物大分子學習的教育門戶
生物大分子學習的教育門戶