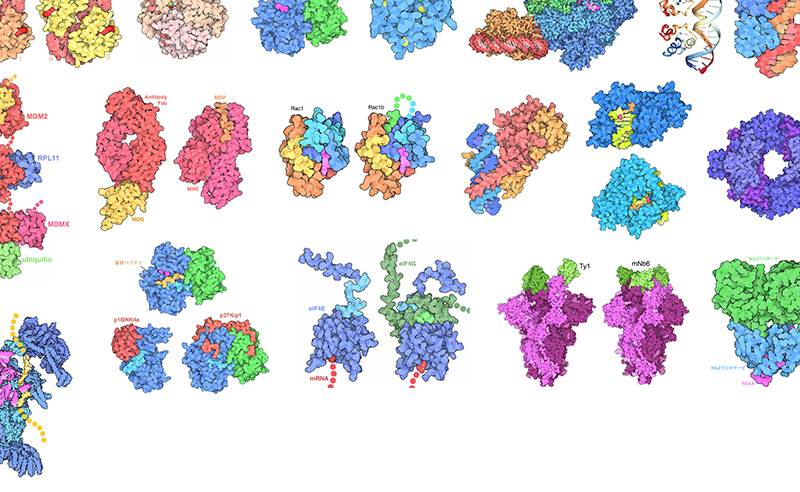
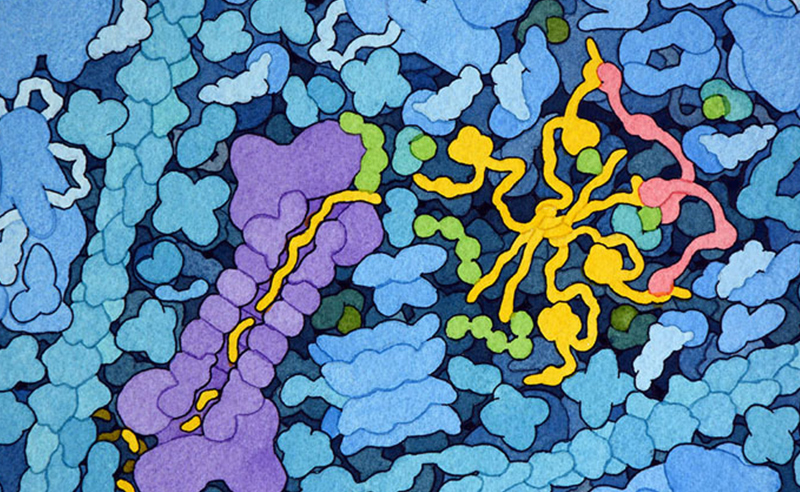
299: 疟原虫 PTEX(Malaria Parasite PTEX)
导致疟疾(malaria)的寄生虫有一个不同寻常的多阶段生命周期。寄生虫由受感染的蚊子携带,并在蚊子叮咬时注入血液。然后,寄生虫感染肝细胞并繁殖。最后,寄生虫逃入血液,侵入红细胞并在其中繁殖。疟疾的大多数症状都是由这一最后阶段引起的,因为寄生虫会使红细胞破裂,并攻击更多的细胞。
有效的效应器
疟原虫进入红细胞后,会分泌数百种蛋白质来重塑细胞。这些效应蛋白具有多种功能,可帮助寄生虫吸收营养和排出废物。它们还能使细胞以有利于寄生虫但不一定有利于受感染者的方式运作,如躲避免疫系统和使受感染的红细胞粘附在血管壁上。PTEX复合体(Plasmodium Translocon of Exported Proteins)将这些效应蛋白从寄生虫体内输送到红细胞中。
寄生虫泵
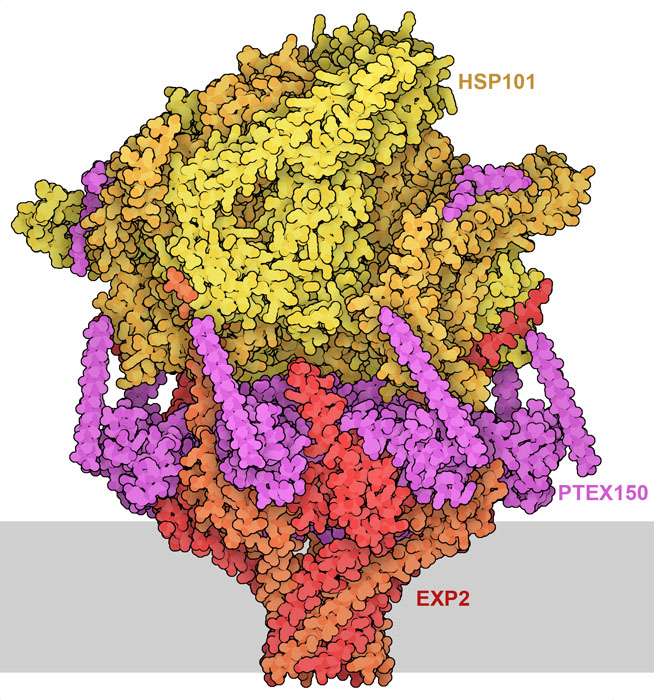
如 PDB ID 6e10的结构所示,PTEX 中心由三部分组成。HSP101是AAA+马达,利用ATP展开效应蛋白并穿过PTEX中心。EXP2在寄生虫膜上开了一个洞,为展开蛋白提供通道。PTEX150将马达与孔连接起来。该结构还包含 HSP101 内运输蛋白的短片段。
粘性细胞
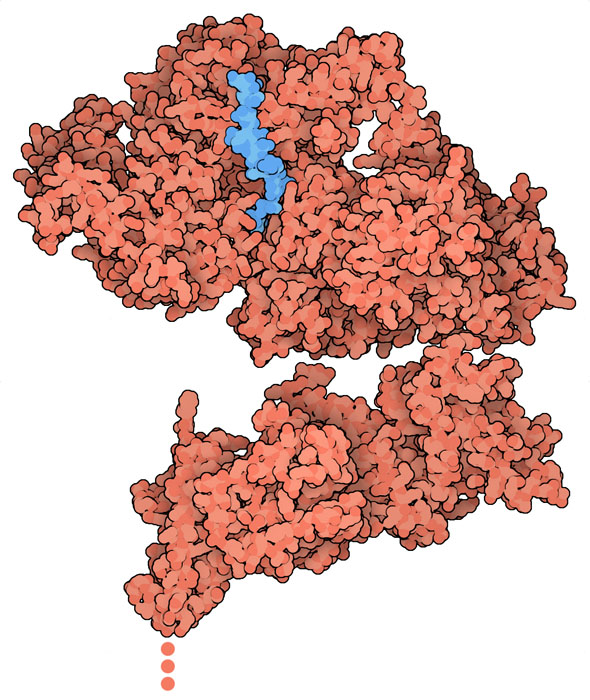
PTEX 释放出一组名为红细胞膜蛋白1(erythrocyte membrane protein 1)的蛋白质,这些蛋白质呈现在红细胞表面,从根本上改变了红细胞的特性。这些蛋白质不会在血液中正常循环,而是将受感染的红细胞粘附在循环系统壁上,将它们固定在一个地方。这对寄生虫来说是一个很大的优势,因为它使它们能够逃避脾脏用于寻找和清除受感染细胞的机制。VAR2CSA(此处显示的是 PDB ID 7jgh和 7nnh结构)是这种寄生虫蛋白家族的成员,它能与胎盘细胞上的分子结合,给母亲和发育中的胎儿带来严重问题。目前正在将这种 VAR2CSA 作为孕妇疟疾疫苗的靶标进行研究。
探索结构
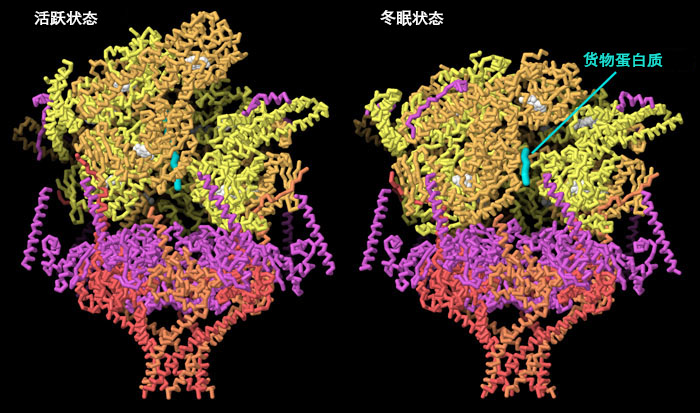
要切换到有互动控制的页面,请点击图表下面的按钮。如果加载没有开始,请尝试点击图表。
PTEX 是一种活性蛋白,在将效应蛋白输送到膜上时会改变形状。两个 PDB 结构捕捉到了这一过程的不同状态:PDB ID 6e10的结构捕捉到了处于不对称状态的 AAA+马达,这在主动泵马达中很常见。在这幅图中,白色显示的是 ATP;PDB ID 6e11的结构捕捉到的是一种更为对称的状态,可能代表了蛋白质的静止状态。点击图下按钮切换到交互式图像,详细查看这些结构。
进一步的讨论议题
- PTEX 中心复合体由多种蛋白质辅助。例如,硫氧还蛋白 2(thioredoxin 2)有助于展开含有半胱氨酸氨基酸的蛋白质。这可以在 PDB ID 3ul3中查看。
参考文献
- 7jgh 2021 Structural basis for placental malaria mediated by Plasmodium falciparum VAR2CSA. Nat Microbiol 6 380-391
- 7nnh 2021 Cryo-EM reveals the architecture of placental malaria VAR2CSA and provides molecular insight into chondroitin sulfate binding. Nat Commun 12 2956-2956
- 6e10, 6e11 2018 Malaria parasite translocon structure and mechanism of effector export. Nature 561 70-75
- 2016 Plasmodium species: master renovators of their host cells. Nat Rev Microbiol 14 494-507
 生物大分子学习的教育门户
生物大分子学习的教育门户